
La técnica, desarrollada por un equipo dirigido por el investigador del CiMUS Marcos García Fuentes en colaboración con el Instituto de Salud Carlos III y la Universidad de Nottingham, está dirigida a mejorar la situación de los enfermos con glioblastoma multiforme (GBM), el tumor cerebral más común y letal y cuya tasa de supervivencia a los cinco años es menor del 5%. Los resultados de esta terapia ensayada con éxito en tumores humanos implantados en ratones se han publicado en la revista ‘Advanced Therapeutics’.
El tratamiento actual para el tumor cerebral más común y letal, el glioblastoma multiforme (GBM), se basa fundamentalmente en la cirugía de extirpación, y logra una supervivencia media de poco más de 14 meses –la supervivencia a los cinco años es menor del 5%–. Sin embargo, esta situación podría mejorar gracias a un nuevo tratamiento desarrollado por un equipo dirigido por el investigador Marcos García Fuentes, investigador del Centro de Investigación en Medicina Molecular y Enfermedades Crónicas (CiMUS) de la Universidad de Santiago, quien ha recibido el apoyo de una Ayuda a Equipos de Investigación en Biomedicina de la Fundación BBVA. El equipo del doctor García Fuentes, en colaboración con el Instituto de Salud Carlos III y la Universidad de Nottingham, ha logrado desarrollar nanopartículas capaces de penetrar los tumores cerebrales y transportar fármacos genéticos al interior de las células cancerígenas. La técnica se ha ensayado con éxito en ratones en un experimento cuyos resultados se han publicado en la revista Advanced Therapeutics.
La utilización de medicamentos capaces de silenciar genes causantes de tumores tiene un enorme potencial para el desarrollo de terapias específicas, personalizadas y efectivas en el tratamiento del cáncer. Sin embargo, estos medicamentos genéticos todavía no tienen una aplicación amplia debido a sus grandes problemas de estabilidad y transporte en el cuerpo. Este complejo camino al interior celular es debido a que los medicamentos genéticos son internalizados a través de vesículas digestivas que degradan su contenido.
Ahora, el equipo dirigido por el doctor García Fuentes ha ensayado el uso de nuevos nanomateriales, denominados polifosfacenos, como vehículos capaces de mejorar el transporte de los medicamentos genéticos contra el cáncer. El estudio de estos materiales ha permitido identificar un derivado que no sólo reduce significativamente la toxicidad de los tratamientos, sino que mejora su transporte al interior de las células y su penetración en tumores. «El secreto de este material –explica García Fuentes- es una estructura que se vuelve ‘insoluble’ en el ambiente ácido de las vesículas digestivas, induciendo su desestabilización y permitiendo al medicamento genético escapar al interior celular».
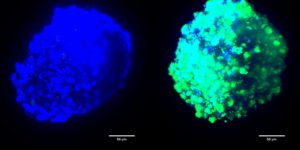
A través de una colaboración con investigadores del Instituto de Salud Carlos III, las nanopartículas terapéuticas fueron cargadas con una secuencia capaz de suprimir células iniciadoras del glioblastoma multiforme. El estudio, realizado en tumores humanos implantados en ratones, ha mostrado que la aplicación del medicamento genético, en combinación con la quimioterapia de primera línea (temozolamida), produce una reducción tumoral mayor que un tratamiento basado únicamente en el fármaco quimioterápico.
«La Ayuda de la Fundación BBVA ha sido muy importante para nosotros, ya que somos un laboratorio pequeño y sin esa financiación no lo hubiésemos podido llevar a cabo. Nos ha permitido seguir una línea de investigación en la frontera del conocimiento y aplicar esta terapia génica, además de darnos más visibilidad tratándose de una ayuda muy competitiva y destinada a investigación de excelencia», señala el investigador.
Implantación directa en el cerebro
El objetivo de este nuevo tratamiento es que se realice como complemento a la cirugía de extirpación y al mismo tiempo que la quimioterapia para conseguir que las células tumorales no se reproduzcan. «La idea es implantarla directamente en el cerebro, por ejemplo, aprovechando la extirpación, porque la vía intravenosa es muy complicada y tiene menos probabilidades de éxito. Las pruebas con ratones han dado resultados muy buenos consiguiendo que los ratones a los que solo se les daba quimioterapia acababan con tumores el doble de grande que los que se trataban con quimioterapia y nanopartículas», apunta García Fuentes.
El investigador añade que, aunque hasta que no realicen ensayos clínicos no lo sabrán con seguridad, los resultados preliminares indican que el efecto de la terapia génica va a estar limitado a una o dos semanas, lo que implicaría que el paciente debería realizar ciclos del tratamiento al igual que se hace con la quimioterapia.
Actualmente, el equipo de investigación dirigido por García Fuentes está trabajando en desarrollos mejorados de la tecnología con vistas a llegar a acuerdos con empresas interesadas en impulsar el desarrollo clínico de la tecnología en el futuro. «Si todo sale bien y logramos el apoyo de empresas, podríamos empezar a realizar los primeros ensayos clínicos en pacientes dentro de cuatro o cinco años», asegura este científico. Además, considera que, una vez verificada su eficacia, la técnica podría utilizarse también para tratar otro tipo de tumores, como el melanoma.
Lee la noticia completa publicada en CiMUS: Crean nanopartículas capaces de penetrar el tumor cerebral más letal y transportar fármacos al interior de las células malignas.
Artículo de referencia: Hsu, Wei-Hsin, et al. Structure-Optimized Interpolymer Polyphosphazene Complexes for Effective Gene Delivery against Glioblastoma. Advanced Therapeutics, 2018, p. 1800126., doi:10.1002/adtp.201800126.
