El Instituto está desarrollando un innovador test diagnóstico del Coronavirus SARS-CoV-2 que permite una detección de secuencias específicas del ARN del virus y puede usarse con mayor facilidad. El desarrollo exitoso de este test permitiría realizar pruebas de alta sensibilidad sin necesidad de disponer de costosos instrumentos y reactivos de laboratorio, como ocurre con los test basados en PCR cuantitativa que requieren, además, personal específicamente formado en dichas técnicas y un tiempo relativamente largo para dar resultados.
El sensor, basado en nanopartículas de oro, es capaz de detectar la secuencia específica del gen RdRP presente en el SARS-CoV-2, así como del gen E común a todos los Coronavirus. El test es básicamente un vial con una disolución acuosa de color rojizo que en presencia del ARN del coronavirus causa una agregación de las nanopartículas de oro funcionalizadas con oligonucleótidos que se precipitan produciendo una disminución clara del color de la disolución que se puede apreciar a simple vista. Esto se debe a una reorganización de cadenas de ADN ancladas en la superficie de la nanopartícula de oro.
El sistema se implementará a 3 sistemas distintos de amplificación con la finalidad de reducir el uso de equipos, personal altamente especializado y reactivos al mínimo:
1) En RT-PCR, evitando el uso de qRT-PCR
2) En amplificación isotérmica, evitando el uso de cualquier tipo de PCR
3) En amplificación no-enzimática, evitando el uso de enzimas y por tanto con una preparación de muestra mínima
Los procesos desarrollados son escalables industrialmente, y se espera adquirir rápidamente la capacidad en IMDEA Nanociencia de producir semanalmente 5.000 sensores basados en nanopartículas.
La (RT-PCR) Reacción en Cadena de la Polimerasa con Transcriptasa Inversa es una variante de la PCR comúnmente usada en biología molecular para generar una gran cantidad de copias de material genético, proceso conocido como amplificación. En la qRT-PCR, el marcaje con compuestos fluorescentes permite la recopilación de datos a medida que la PCR avanza por lo que ofrece muchos beneficios, como que se pueden detectar simultáneamente muchos blancos en cada muestra, pero esto requiere la optimización y el diseño de una sonda específica.
El ISCIII ha concedido a la Fundación Instituto Madrileño de Estudios Avanzados en Nanociencia una ayuda por importe de 340.000,00 euros del fondo “Para subvenciones de concesión directa para proyectos y programas de investigación del virus SARS-CoV2, causante del COVID-19”, del presupuesto de gastos del ISCIII para el año 2020 (FONDO – COVID19) con el fin de contribuir a validar este sensor que IMDEA Nanociencia está desarrollando.
La propuesta financiada resulta adecuada a la situación de urgencia, permitiendo y una implementación y puesta en marcha inmediata en el Sistema Nacional de Salud, con resultados concretos, tempranos y oportunos a la situación actual. Asimismo, da respuesta al interés social que motiva la presente concesión, contribuyendo a un mejor diagnóstico clínico de pacientes del SNS infectados por SARS-CoV-2.
Los sistemas propuestos tendrían una implantación rápida y sencilla en los procedimientos actuales de diagnóstico, y se han enunciado de mayor a menor necesidad de recursos. El primer sistema solo requiere de un termociclador, el segundo de un termobloque, y el tercero no requeriría enzimas. Por tanto, su implementación podría realizarse no solo en todos los hospitales sino en los centros de salud. La rapidez en la obtención de los resultados (unas pocas horas) por un cambio de color perceptible a simple vista, es otra de las grandes ventajas de estos sistemas.
En el instituto podemos preparar nanopartículas, oligonucleótidos y tiras de nitrocelulosa modificadas a una escala pequeña. De hecho, hemos iniciado un proyecto industrial con la empresa Synthelia Organics para la preparación en flujo de nanopartículas. Para la síntesis de oligonucleótidos en mayores cantidades, solicitamos presupuesto para la adquisición de un equipo nuevo. Respecto a los sensores de tira, necesitaríamos un dispensador automático. Con este equipamiento IMDEA Nanociencia podría producir unos 5.000 sensores a la semana mediante procesos escalables industrialmente, por lo que el sistema descrito podría prepararse en un orden de magnitud mayor por la industria.
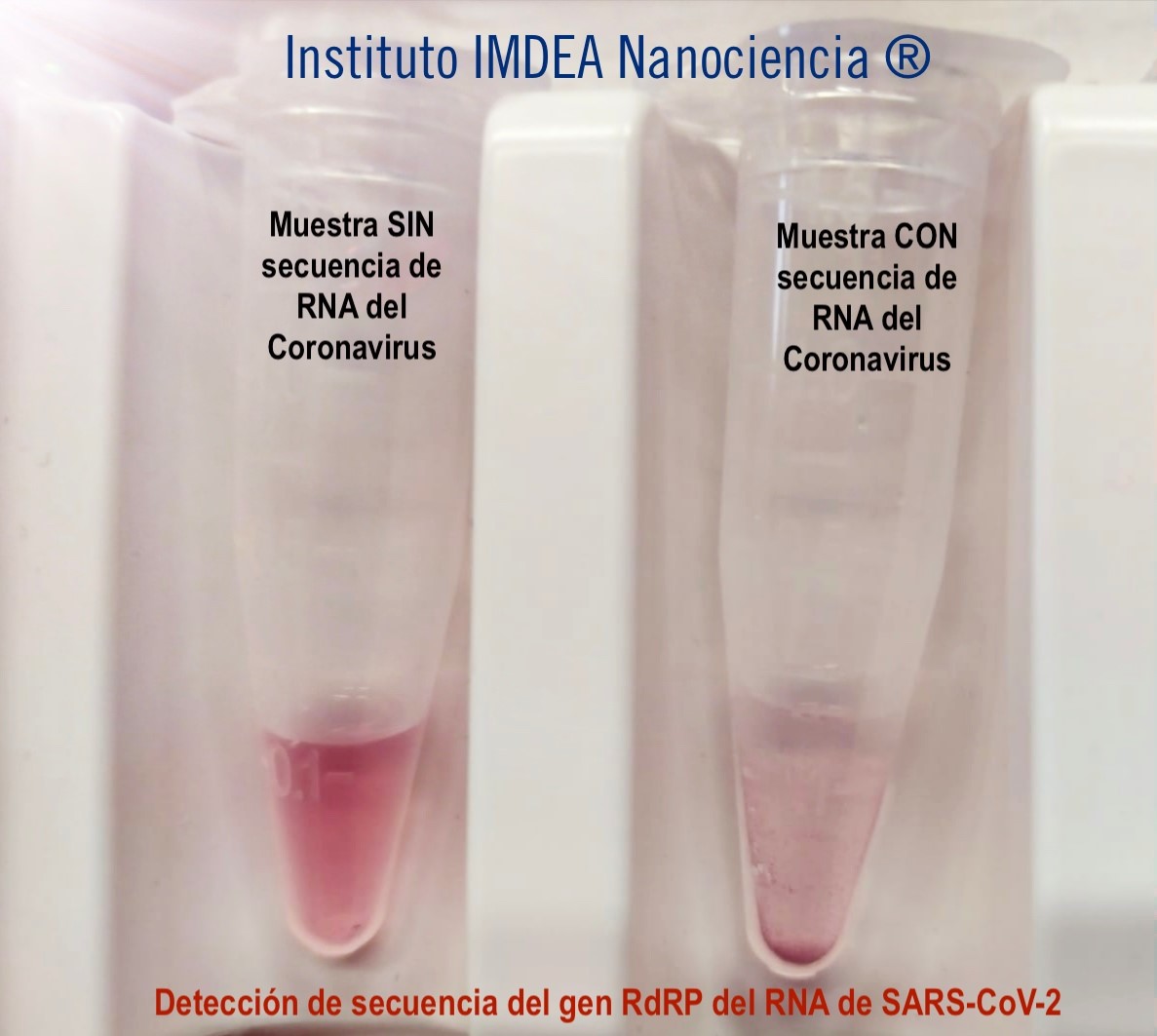
Según explica el Dr. Álvaro Somoza, responsable del equipo que desarrolla el test: Las cadenas de ADN presentes en la superficie de las nanopartículas están plegadas en forma de horquilla y tienen un grupo hidrofóbico en el extremo. En esta disposición la estructura es soluble en agua, pero en presencia del ARN de virus, la horquilla se abre y el colesterol se expone al medio, dando lugar a una estructura insoluble en agua y provocando la precipitación de las nanopartículas.
Entre las medidas más evidentes para la contención del virus SARS-CoV-2, responsable de la enfermedad Covid19 se incluye su detección. Identificar a portadores del virus y, por tanto, vehículos potenciales para su transmisión, es vital, no sólo en pacientes que muestran los síntomas, sino, fundamentalmente, en pacientes asintomáticos, pero igualmente infecciosos. De esta manera sería posible aislarlos y prevenir la expansión del virus. Para ello es necesario evaluar a un gran porcentaje de la población, y repetir esos estudios durante varias semanas, ya que el virus puede ser trasmitido de persona a persona desde varios días antes de que aparezcan los primeros síntomas (si aparecen), y hasta más de tres semanas desde el momento del contagio.
La detección del virus se hace actualmente mediante dos metodologías. La más directa y, por tanto, más fiable de las dos requiere el uso de un equipamiento sofisticado y de personal formado adecuadamente. Este sistema se conoce como qRT-PCR, e implica la transcripción inversa del ARN del virus para convertirlo en ADN, la amplificación del ADN mediante la técnica de PCR, y la cuantificación, en el mismo equipo, mediante la utilización de unas sondas fluorescentes. Este proceso suele llevar varias horas desde la obtención de la muestra, la cual tiene que trasladarse a los centros donde dispongan de los equipos y el personal necesarios para realizar este proceso, así como de los requerimientos de bioseguridad pertinentes. En muchos casos, dada la escasez de equipos PCR, este traslado supone incluso el traslado de las muestras de una Comunidad Autónoma a otra.
El sistema qPCR es muy sensible, y permite detectar el ARN del virus, aunque esté presente en pequeñísimas cantidades, por lo que es muy útil para poder detectarlo en fases iniciales de la enfermedad, así como para confirmar cuándo el paciente está libre de virus. Actualmente es el método de referencia, aunque cada país está utilizando una región ligeramente distinta del ARN del virus para la detección. En la Comunidad de Madrid se utiliza el método descrito por Dr. Christian Drosten del Instituto de Virología Charité en Berlín.
El otro método implica el uso de anticuerpos, y se puede diseñar de dos formas distintas: i) para la detección de proteínas del virus o ii) los anticuerpos frente a los virus generados por el paciente. Estos sistemas diagnósticos son conocidos como test rápidos, y sus principales ventajas son la facilidad de uso y la rapidez en obtener un diagnóstico en unos 15 min. Sin embargo pueden presentar varios problemas, ya que la detección será eficiente cuando el virus esté presente en una concentración relativamente alta, en el primer caso, o cuando los anticuerpos desarrollados por el paciente se encuentren en sangre a unos niveles óptimos. Por lo general se tarda varios días en alcanzar estos niveles (7-14 días, en promedio para pasar de un 40% a un 100%), lo que puede no ser muy eficaz, ya que los pacientes infectados pueden transmitir la enfermedad, incluso tener síntomas evidentes, y no dar positivo en el test si éste no tiene sensibilidad suficiente. Además, este tipo de test puede no ser adecuado en pacientes inmunocomprometidos.
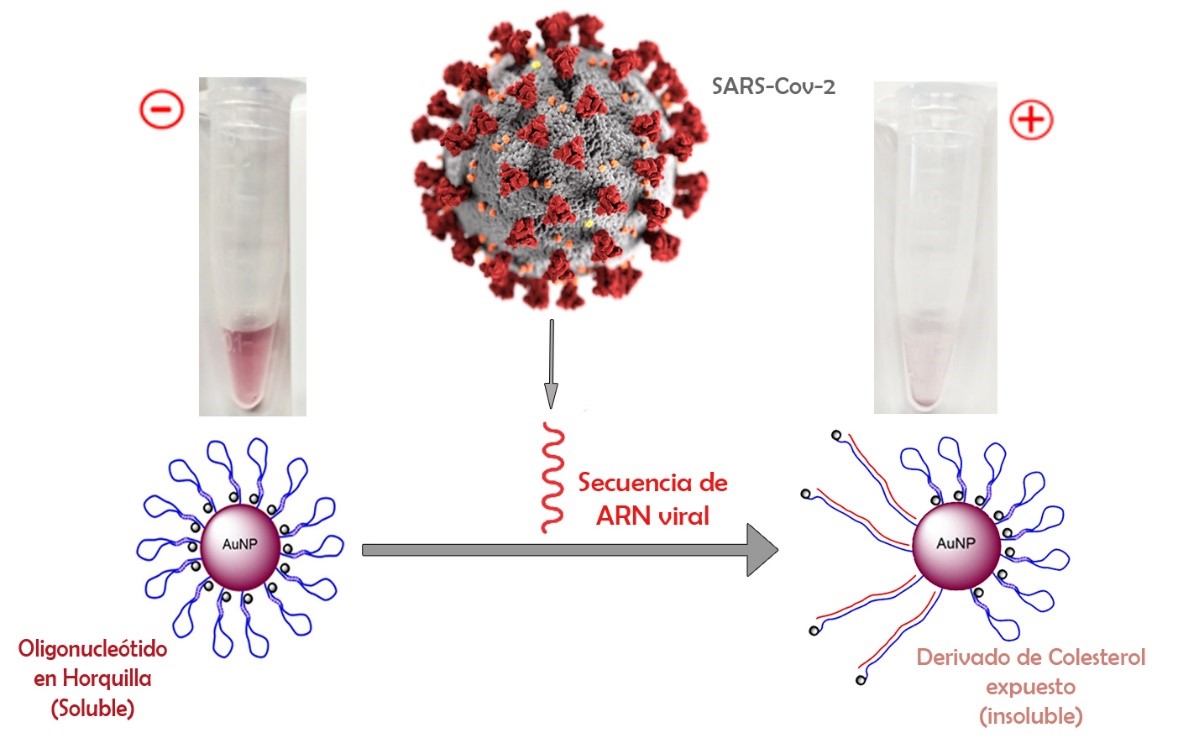 Por estos motivos, en IMDEA Nanociencia estamos desarrollando un test diagnóstico que combine ambos conceptos, es decir: que permita una detección de secuencias específicas del ARN del virus, pero que no requiera de los equipos de qRT-PCR, y pueda usarse con facilidad. El sensor tiene un diseño capaz de detectar la secuencia específica del gen RdRP presente en el SARS-CoV-2, así como del gen E, común a todos los Coronavirus.
Por estos motivos, en IMDEA Nanociencia estamos desarrollando un test diagnóstico que combine ambos conceptos, es decir: que permita una detección de secuencias específicas del ARN del virus, pero que no requiera de los equipos de qRT-PCR, y pueda usarse con facilidad. El sensor tiene un diseño capaz de detectar la secuencia específica del gen RdRP presente en el SARS-CoV-2, así como del gen E, común a todos los Coronavirus.
Según el Prof. Miranda, Director del Instituto e Investigador Principal del Proyecto financiado por el ISCIII: La investigación en Nanociencia desarrollada en el Instituto en estos años ha producido varios avances biomédicos que son ya una realidad. Esperamos poder contribuir también en la lucha contra esta pandemia. Estamos reorientando una parte importante de las capacidades multidisciplinares del Instituto para lograr un test eficiente y simple de usar.
Fuente: IMDEA
