Las nanovesículas, conocidas como quatsomas, que se han diseñado para encapsular y administrar microRNA para el tratamiento de tumores. Este estudio, publicado en Small, es destacado en el número especial de Women in Materials Science de la revista Advanced Materials.

Los microARN (también conocidos como miARNs) son pequeñas moléculas de ARN que pueden interferir con la estabilidad de otras moléculas de ARN (particularmente, el ARN mensajero). Tienen un gran potencial terapéutico debido al papel central que juegan en desarrollo de múltiples enfermedades. Sin embargo, estas moléculas todavía se usan de forma muy poco frecuente en pacientes debido a su inestabilidad en el torrente sanguíneo y su poca capacidad de llegar a tejidos específicos. Una estrategia potencial para mejorar la administración clínica de miRNA en el cuerpo es encapsularlo en transportadores diminutos que permitan superar las barreras actuales de administración de los miARNs, sin efectos secundarios y que ofrezcan otras funciones complementarias.
Para ello, se ha desarrollado una nanoestructura, conocida como quatsoma, compuesta por dos membranas lipídicas, mejorada y diseñada especialmente para esta aplicación. En la publicación en Small, destacada en el número “Women in Materials Science” de la revista Advanced Materials, se presenta una nueva formulación de quatsomas con una estructura, composición y sensibilidad al pH controlables.
El estudio es el resultado de un trabajo de un equipo multidisciplinar formado por investigadores del Instituto de Ciencia de Materiales de Barcelona, ICMAB-CSIC, el Vall d’Hebron Research Institute (VHIR)-UAB, el Instituto de Bioingeniería de Catalunya (IBEC), el Barcelona Institute of Science and Technology (BIST), la red CIBER de Bioingeniería, Biomateriales y Nanomedicina (CIBER- BBN), la empresa Nanomol Technologies SL, el Technion-Instituto de Tecnología de Israel y el Instituto de Sistemas Moleculares Complejos (ICMS).
“En este estudio hemos colaborado con hospitales, redes de investigación y empresas. Los resultadoa obtenidos ilustran la importancia de la colaboración entre campos y más allá del sistema académico”, dice Ventosa.
Estos nuevos quatsomas pueden conjugarse con miARNs capaces de inducir una supresión tumoral e inyectarse por vía intravenosa para liberar los miARNs en tumores primarios de neuroblastoma o en los sitios frecuentes de metástasis, como el hígado o el pulmón, llegando con mayor éxito y estabilidad que si el miARN se inyectara solo. Una vez liberado, el miRNA tiene un efecto sobre la proliferación celular y los genes relacionados con la supervivencia en los tumores, lo que reduce la tasa de crecimiento del tumor.
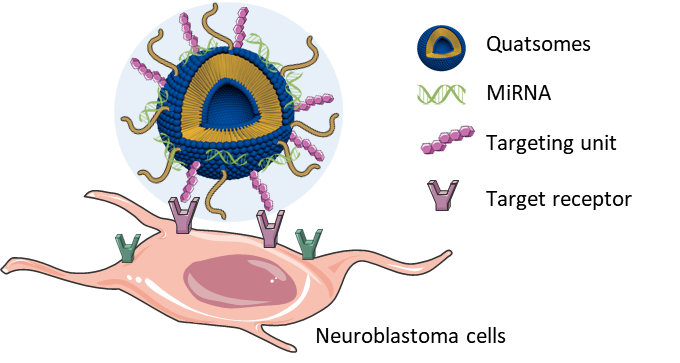
Estas nanovesículastienen unas propiedades óptimas para encapsular microARN: tienen un tamaño inferior a 150 nanómetros y son estables en una solución líquida durante más de 6 meses; también tienen una sensibilidad al pH ajustable, lo que significa que diferentes niveles de pH pueden desencadenar diferentes respuestas.
La producción de estas nanovesículas se ha optimizado pensando en su aplicación final y para garantizar su uso en ensayos clínicos y con pacientes. Utilizando una metodología respetuosa con el medio ambiente y escalable de un solo proceso, llamado DELOS, los investigadores han diseñado un producto producido bajo condiciones de Buenas Prácticas de Manufactura (GMP) establecidas por la Unión Europea. “Es el momento de trasladar nuestros hallazgos científicos a la práctica clínica para ofrecer un beneficio a los pacientes” dice Ariadna Boloix, investigadora del VHIR.
En este estudio se demuestra la funcionalidad de los quatsomas en la administración de miARN para el tratamiento del neuroblastoma, un tumor extracranial del sistema nerivoso periférico que es responsable de aproximadamente el 15 % de todas las muertes por cáncer pediátrico. Los resultados muestran que los quatsomas protegen el miARN de la degradación por enzimas presentes en el torrente sanguíneo y favorecen su acumulación en tejidos como el hígado, el pulmón y los tumores subcutáneos entre otros tejidos.
Artículo de referencia: Engineering pH-Sensitive Stable Nanovesicles for Delivery of MicroRNA Therapeutics
Ariadna Boloix, Natalia Feiner-Gracia, Mariana Köber, Javier Repetto, Rosa Pascarella, Aroa
Soriano, Marc Masanas, Nathaly Segovia, Guillem Vargas-Nadal, Josep Merlo-Mas, Dganit Danino,
Inbal Abutbul-Ionita, Laia Foradada, Josep Roma, Alba Córdoba, Santi Sala, Josep Sánchez de
Toledo, Soledad Gallego, Jaume Veciana, Lorenzo Albertazzi, Miguel F. Segura*, Nora Ventosa*
Small, 18, 3, 2022 DOI: 10.1002/smll.202101959
Fuente: ICMAB
